Лечение онкологических заболеваний на сегодняшний день подразумевает уничтожение опухоли всеми возможными способами. Но почему бы не «усыпить» клетки ...
Читать далее
Еще в 2016 году, когда FDA включило зеленый свет для клинических испытаний метморфина — препарата, который увеличивал продолжительность жизни на 40% у животных моделей, — стало понятно, что происходит смена парадигмы нашего отношения к старению и продолжительности жизни. Старение — до сих пор неизбежная часть жизнь — может быть болезнью. И как болезнь, его можно «лечить» — откладывать, останавливать или даже обращать вспять — при наличии подходящих лекарств.
Решение FDA стало кульминацией ряда первоклассных исследований животных — и вполне успешных — целью которых было обратить вспять распад тканей у старых грызунов. Кровь молодых, метморфин и сенолитики — препараты, уничтожающие «протекающие» старые клетки — перезагружали стареющие кости, сердца и мозги у старших представителей рода грызунов. И они не просто становились здоровее — они жили дольше.
Благодаря многочисленным методам лечения, связанным с болезнями старости, и неизменному интересу (и финансированию) от частного сектора, импульс в этой области никак не исчезает. Когда же мы поборем старость раз и навсегда?
Не так быстро, говорит доктор Пол Нельсон и его коллега Джоанна Мазел из Аризонского университета.
Применяя концепцию эволюции к клеточным обитателям наших тел, ученые построили математическую модель, которая изучает поведение клеток по мере старения. И новости не очень хорошие.
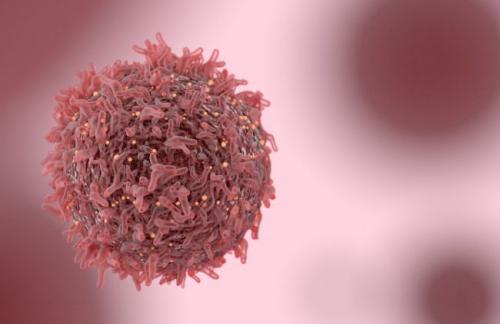
Со старением популяция здоровых клеток истощается. Некоторые постепенно теряют свои нормальные функции, перестают делиться и входят в зомбиподобное состояние — становятся сенесцентными. Другие мутируют, приобретая способность делиться и размножаться бесконтрольно, становятся раковыми.
Как оказалось, избавление от обоих типов проблемных клеток невозможно.
«Математически старение неизбежно — то есть неизбежно по своей сути. Нет никакой логической, теоретической и математической возможности избежать его», говорит Мазел. Свою работу ученые опубликовали в PNAS.
Мир клетки
Наши клетки — как главные герои антиутопии: они рождены в суровом обществе, в котором каждому уготована своя роль, и по мере старения и утраты функций, как в часовом механизме, они следуют генетической программе, которая приказывает им совершать суицид ради высшей цели — блага организма, который они составляют.
В некотором смысле эти клетки живут в полицейском государстве в состоянии постоянной борьбы: здоровые клетки борются со стареющими за пространство и пищу, благодаря чему общество — ткани и органы — управляется здоровыми членами и работает безотказно. Жизнь этих стареющих клеток — лишь небольшая цена.
Но иногда стареющие клетки дают отпор. Меняя экспрессию генов, они получают возможность делиться и распространяться. Эти раковые клетки обманывают систему: вместо кооперации во имя высшей цели, они все вредят организму, который населяют.
В какой-то момент многоклеточный организм вроде человека обзаведется как сенесцентными клетками, так и раковыми, объясняют авторы работы.
Незаконченная борьба
Поскольку каждая клетка питается собственным набором экспрессированных генов — генов, которые превращаются в белки, — мы можем рассматривать их как общество из разных людей в состоянии напряженной конкуренции.
Подобно тому, как ученые изучают, как генетические изменения видов приводят к их эволюции, ученые также могут использовать аналогичные базовые принципы для отслеживания поведения клеток, когда те сталкиваются с изменяющейся средой, например, когда мы стареем.
«Когда люди пытаются ответить на вопрос: «почему в процессе эволюции появилось старение?», они обычно спрашивают: «почему у нас есть гены, которые заставляют нас стареть?». В этом вопросе подразумевается, что могут быть гены, которые не дадут нам постареть», и отдельные клетки могут располагать нужной комбинацией генов, которые позволят им оставаться здоровыми и бессмертными, объясняют авторы.
Современные теории эволюции старения подразумевают, что старение можно остановить, если конкуренция будет достаточно сильной, чтобы устранить нездоровые и опасные клетки — то есть сенесцентные и раковые.
Другими словами, ученые предположили, что мы стареем, потому что давление естественного отбора не идеально: эволюция на клеточном уровне не выполняет свою работу.
Именно это вознамерились проверить авторы работы.
Модель старения
Ученые начали с простой идеи: клетки не могут быть одновременно сенесцентными и раковыми длительное время. «Раковые мутации представляют изменения в чертах, которые регулируют клеточный цикл и заставляют клетку нарушать правила и делиться, когда она не должна, либо отказываться умирать, когда она должна бы», говорят они.
Эти мутации усиливают стойкость клетки, но снижают ее способности к кооперации — в конце концов, раковые клетки не очень хорошо функционируют.
И напротив, мутации, которые приводят к сенесцентности, по большей части вмешиваются в метаболизм клетки, заставляя ее останавливать рост. Стареющие клетки теряют свою стойкость, но умирая, они сотрудничают до конца.
Чтобы увидеть, как конкуренция меняет траекторию эволюции клетки, ученые использовали общую, абстрактную математическую систему, которая показала, как клетки развиваются с течением времени в зависимости от их текущего состояния.
К примеру, при старении в клетках накапливаются скопления белка, что снижает их общую функцию и здоровье. Это и другие вредные события приводят к изменениям в уровне стойкости и кооперации клеток, что, в свою очередь, влияет на здоровье и продолжительности жизни организма.
Нельсон и Мазел не считают мутации хорошими. Важное допущение в нашей модели таково, что организм будет ухудшаться с возрастом, говорят они. Некоторые ученые предположили, что если инструменты ремонта клеток будут достаточно сильны, идеально здоровый геном можно было бы поддерживать бесконечно, но эти механизмы ремонта сами по себе неизбежно будут ухудшаться.
Решение этой модели приводит к «неудобной правде»: конкуренция между клетками — это палка о двух концах, но отсутствие конкуренции приводит к устойчивой деградации.
Когда клетки конкурируют за ресурсы, сенесцентные клетки эффективно уничтожаются и заменяются здоровыми, но мутации, которые приводят к раку, распространяются. Это приводит к ухудшению здоровья организма, поскольку кооперация снижается.
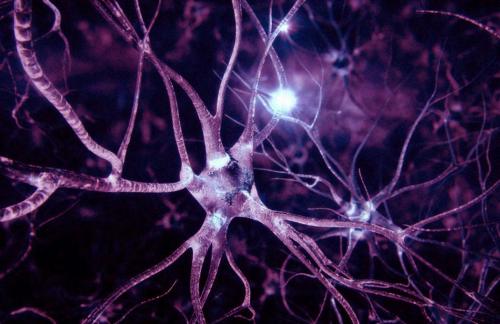
Если клетки не конкурируют — например, в тканях, где они целиком созрели и перестали делиться, вроде нейронов — нездоровые клетки не могут заменяться, и организму становится хуже, поскольку он наполняется старыми, нефункциональными клетками.
Выходит, «конкуренция или ее отсутствие между клетками может избавить нас либо от рака, либо от стареющих клеток, но не от обоих. И пока вы держите одну проблему под контролем, другая становится хуже», говорят он.
Пища для размышлений
Если вы приуныли, не все так плохо.
Хотя модель ученых гласит, что старение неизбежно, она не исключает возможность замедления процесса.
«У нас, вероятно, есть много пагубных черт, которые приводят нас к старению и преждевременной смерти», и укрощение этих черт может «радикально» задержать процесс, пусть и не устранить его полностью, считают ученые. Их теория может даже помочь в борьбе против старения.
Взять сенолитики, например, которые нацеливаются и убивают старые клетки-зомби. Хотя исследования грызунов с использованием этих препаратов не задокументировали увеличение числа случаев рака, риск остается. Модель ученых показывает, что такого рода лечение приведет к кратковременному снижению симптомов старения, за которым последует повышенный риск развития рака, поскольку вы просто поощряете кучку клеток к началу распространения.
Старение — это динамический процесс, когда раковые и стареющие клетки меняются вместе, поэтому невозможно решить одну проблему, не давая пространство для развития второй.